UNA SINTESI DELLE NUOVE LINEE GUIDA WSAVA SULLA VACCINAZIONE DI CANE E GATTO
A distanza di otto anni dalla loro terza edizione (Day et al., 2016), sono state pubblicate le linee guida WSAVA 2024 sulla vaccinazione del cane e del gatto (Squires et al., 2024). Il nuovo gruppo di esperti (Vaccination Guidelines Group, VGG) che si è cimentato nella redazione delle linee guida WSAVA 2024 – rinnovatosi per tre quarti rispetto alla precedente edizione – è composto da 4 autori rappresentativi delle realtà americana, australiana ed europea.
In queste nuove linee guida sono stati confermati alcuni punti fermi ed apportate modifiche che assecondano la necessità di aggiornamento bibliografico, riducendo sempre più i riferimenti ad esperienze ed opinioni personali.
Restano punti fermi
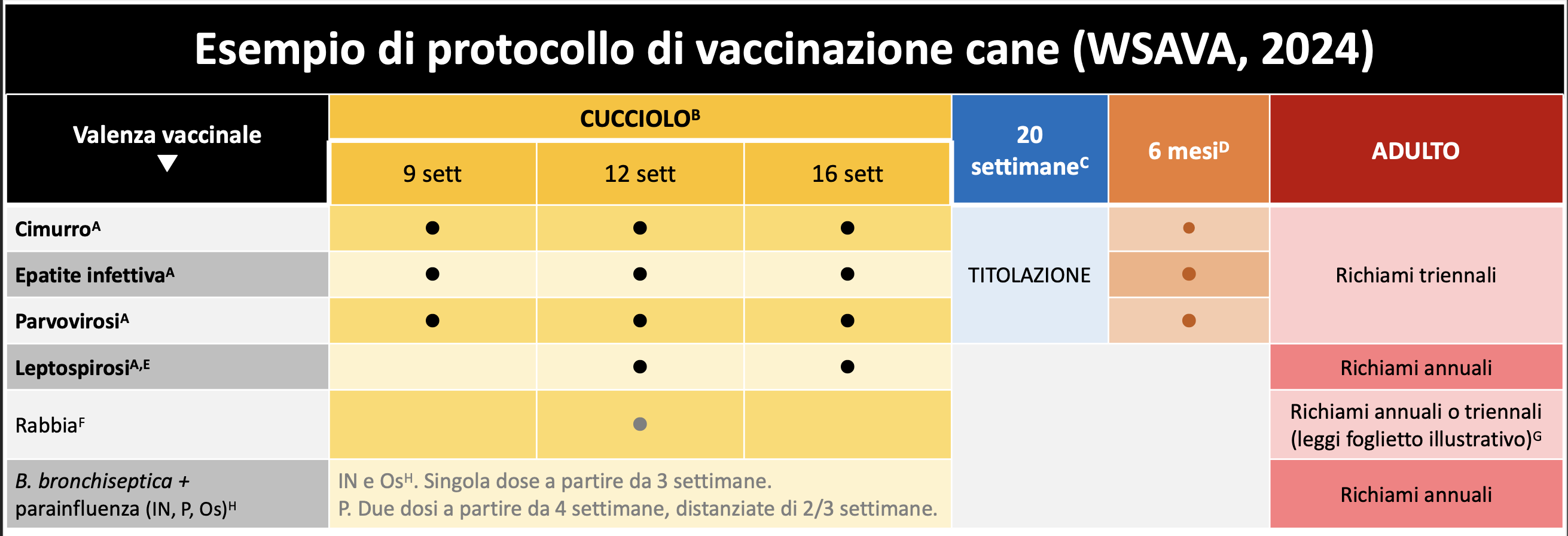
1) la chiusura del primo ciclo di vaccinazione del cane e del gatto non prima delle 16 settimane di età
2) l’attribuzione di valenze “core” ai vaccini contro la parvovirosi, l’epatite infettiva e il cimurro nel cane e contro la panleucopenia, la rinotarcheite infettiva e la calicivirosi nel gatto
3) la raccomandazione di vaccinare quanti più cani e gatti possibili con i vaccini “core”, ma al contempo
4) di ridurre il carico vaccinale sui singoli soggetti, non somministrando più vaccini di quanto necessario. Al fine di implementare quest’ultimo punto, si continuano a suggerire la vaccinazione triennale per le valenze virali “core” e la titolazione anticorpale.
Al fine di implementare quest’ultimo punto, si continuano a suggerire la vaccinazione triennale per le valenze virali “core” e la titolazione anticorpale.
In merito alla triennalità, resta confermata l’eccezione di ricorrere all’annualità per le valenze herpesvirus e calicivirus nei gatti esposti ad alto rischio. Un’indicazione simile viene data per il vaccino contro il virus della leucemia felina (FeLV, vedi dopo).
Per quanto riguarda la titolazione anticorpale, si continua a suggerirla 4 settimane dopo la chiusura del primo ciclo di vaccinazione, a conferma dell’avvenuta immunizzazione verso le valenze virali “core” del cane e verso la panleucopenia del gatto.
Inoltre, si raccomanda la titolazione anticorpale anche in tutta una serie di circostanze (animali immunodepressi, animali con malattie autoimmunitarie, ecc) nelle quali la vaccinazione potrebbe risultare problematica. Il VGG accenna anche alla possibilità di offrire la titolazione anticorpale in alternativa al richiamo vaccinale triennale; tuttavia, alla luce di quanto emerso nella recente letteratura a proposito dei kit rapidi, si tende a prediligere l’invito a ricorrere ai metodi “gold standard” di titolazione anticorpale.
Le modifiche più importanti rispetto alla precedente edizione hanno riguardato i vaccini contro la leptospirosi canina e contro la leucemia felina, oltre ad un più stringente invito ad anticipare il richiamo vaccinale che, tipicamente, viene ancora effettuato ad un anno di età o ad un anno dopo l’ultimo vaccino di primo ciclo.
Quanto ai vaccini contro la leptospirosi canina, la leucemia felina e la rabbia, considerati in passato vaccini “non-core”, il VGG ha inteso identificare delle condizioni in cui questi vaccini meritano di essere elevati al rango di vaccini “core”.
Per la leptospirosi canina, il suggerimento è stato quello di considerare “core” il vaccino nei paesi o nelle regioni in cui la malattia è endemica, dove sono noti i sierogruppi implicati e dove sono disponibili vaccini idonei.
La necessità di fare questo distinguo, tra le diverse realtà territoriali, per stabilire se ritenere o meno “core” questo vaccino, nasce dal fatto che gli attuali vaccini non garantiscono un’adeguata protezione verso tutti i sierogruppi. Sostanzialmente, non si può attribuire la valenza “core” ad un vaccino, se non sappiamo verso quali sierogruppi dobbiamo proteggere o se il vaccino è privo delle valenze necessarie a proteggere verso i sierogruppi ai quali i cani sono esposti. In futuro, lo sviluppo di vaccini capaci di proteggere contro la maggior parte delle varianti patogene conosciute, permetterà di risolvere questi dilemmi e di estendere le regioni del mondo in cui i vaccini contro la leptospirosi potranno essere considerati “core”.
A tal proposito, in considerazione degli studi epidemiologici pubblicati (Tagliabue et al., 2016; Bertasio et al., 2020) e dei vaccini disponibili (bivalenti, trivalenti e tetravalenti), si può ritenere l’Italia tra i paesi nei quali considerare “core” il vaccino contro la leptospirosi canina.
In merito alla leucemia felina, il VGG ha adottato il suggerimento, già proposto nelle linee guida americane (Stone et al., 2020), di considerare “core” il vaccino FeLV nei gatti di meno di un anno di età.
Questa raccomandazione è stata estesa anche ai gatti adulti che hanno accesso all’esterno, o che hanno contatti con gatti che vivono all’esterno. Invece, in quelle regioni del mondo dove la malattia è rara o riportata raramente in gatti di importazione, la vaccinazione contro la leucemia felina deve ancora essere considerata “non-core”.
Per quanto riguarda la rabbia, la promozione a vaccino “core” riguarda cani e gatti che vivono in aree endemiche o nelle quali la legislazione locale impone l’obbligo di vaccinazione. Questo “upgrade” si è reso necessario perché la precedente classificazione del vaccino contro la rabbia come “non-core” rischiava di fare sottovalutare, nelle aree endemiche, l’importanza della vaccinazione contro una malattia letale di cane e gatto, che, tra l’altro, presenta un impatto importante sulla sanità pubblica.
Terza ed ultima modifica significativa rispetto alla precedente edizione è il più stringente invito ad anticipare ai 6 mesi di età, il richiamo delle valenze vaccinali “core” di origine virale (con l’eccezione del vaccino FeLV, per il quale anche quando considerato “core”, si suggerisce richiamo dopo un anno).
Il fine, è quello di evitare che i pochi soggetti non immunizzatisi nel primo ciclo di vaccinazione, restino scoperti fino all’anno di età, in attesa del richiamo vaccinale.
In conclusione, vale la pena ricordare che lo spirito con il quale sono state redatte le linee guida WSAVA per la vaccinazione del cane e del gatto non è quello di descrivere standard obbligatori e/o minimi di profilassi, ma piuttosto quello di fornire informazioni utili ad agevolare il processo decisionale dei medici veterinari. Ricordiamo ancora una volta che la vaccinazione è un atto medico-veterinario e che non esistono protocolli vaccinali “buoni per tutte le stagioni”, ma ogni cane e gatto deve essere vaccinato tenendo in debita considerazione una serie di fattori variabili, quali la situazione epidemiologica, lo stile di vita, la presenza di particolari condizioni fisiologiche o patologiche.
In allegato un PDF con gli schemi semplificati dei protocolli vaccinali aggiornati secondo le nuove linee guida.
References
Bertasio et al. Detection of New Leptospira Genotypes Infecting Symptomatic Dogs: Is a New Vaccine Formulation Needed? Pathogens 2020, 9, 484; doi:10.3390/pathogens9060484
Day et al. Guidelines for the vaccination of dogs and cats. Small Anim Pract. 2016; 57(1):4-8. doi: 10.1111/jsap.12431
Ellis et al. 2022 AAHA Canine Vaccination Guidelines. J Am Anim Hosp Assoc. 2022; 58(5):213-230. doi: 10.5326/JAAHA-MS-Canine-Vaccination-Guidelines.
Squires et al. 2024 guidelines for the vaccination of dogs and cats - compiled by the Vaccination Guidelines Group (VGG) of the World Small Animal Veterinary Association (WSAVA). J Small Anim Pract. 2024; 65(5):277-316. doi: 10.1111/jsap.13718
Stone et al. 2020 AAHA/AAFP Feline Vaccination Guidelines. J Am Anim Hosp Assoc 2020; 56:249–265. doi 10.5326/JAAHA-MS-7123
Sykes et al. Updated ACVIM consensus statement on leptospirosis in dogs. J Vet Intern Med 2023; 37(6):1966-1982. doi: 10.1111/jvim.16903.
Tagliabue et al. Serological surveillance of Leptospirosis in Italy: two‑year national data (2010‑2011). Veterinaria Italiana 2016, 52 (2), 129-138. doi: 10.12834/VetIt.58.169.2
Domenico Russo, Medico Veterinario, PhD, Key Account Manager Mylav
Nicola Decaro, Medico Veterinario, PhD, Diplomato ECVM, EBVS® – European Specialist in Veterinary Microbiology, Professore Ordinario di Malattie Infettive dell'Università di Bari, Esperto in Malattie infettive e Microbiologia di Mylav
Commenti
- Nessun commento trovato








Lascia i tuoi commenti
Login per inviare un commento
Posta commento come visitatore